Menu
Periodiek Systeem Der Elementen
Het periodiek systeem der elementen ( afgekort PSE ) is een systematische ordening van de chemische elementen in een tabel, die is gebaseerd op de bouw van de atomen en de daaruit voortvloei-ende fysische en chemische eigenschappen van de elementen. Reeds in 1817 ontdekte J.W. Dödereinereen zekere regelmaat in de eigenschappen van chemische elementen. Het duurde echter tot 1869 voor D.J. Mendelejev en J.L. Meyer ( onafhankelijk van elkaar ) een periodiek systeem opstelden dat alle toen bekende elementen omvatte. In het systeem van Mendelejev waren bovendien nog plaatsen opengehouden voor elementen die toen nog niet bekend waren, dit systeem geldt, met enige verbeteringen en aanvullingen, tot op de huidige dag. De bouw van atomen kan eigenlijk alleen beschreven worden met behulp van wiskundige formules, zonder dat daaraan een concrete voorstelling verbonden is. Men maakt gebruik van atoommodellen om atoomfysische begrippen enigszins te verduidelijken. Met het hier gebruikte schillenmodel kunnen al veel van de chemische en fysische eigenschappen van atomen worden verklaard vanuit hun plaats in het PSE; voor het beschrijven van het golfkarakter van materiedeeltjes moet echter een quantum mechanisch atoomodel worden gebruikt.
|
De elementen zijn in het PSE enerzijds gerangschikt naar opklimmend atoomnummer ( d.i. het aantal protonen in de atoomkern van een element ), anderzijds naar de elektronenconfiguratie : het aantal elektronen is gelijk aan het aantal protonen, maar hun banen kunnen op diverse wijzen over de verschillende schillen rond de atoomkern zijn verdeeld. Deze schillen hebben meestal ook verschillende energieniveaus, de elektronenconfiguratie is bepalend voor de chemische en fysische eigenschappen van een element. Het PSE is onderverdeeld in perioden en in groepen. In de groepen zijn ee-menten samengevoegd waarvan de chemische eigenschappen ( door een vergelijkbare elektronenconfiguratie ) grote gelijkenis vertonen.
|
Er wordt onderscheid gemaakt tussen hoofdgroepen ( a ) en nevengroepen ( b ), waarbij de hoofdgroepen vaak genoemd zijn voor de groep.
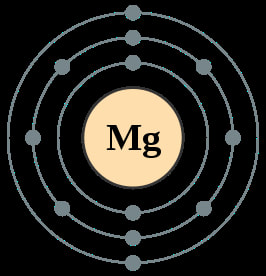
De eerste hoofdgroep omvat de alkalimetalen ( lithium, natrium, kalium, rubidium, cesium en francium ); de tweede hoofdgroep de aardkalimentalen ( beryllium, magnesium, calcium, strontium, barium, radium ). De derde hoofdgroep wordt aangeduid als de aarden , de vierde als koolstofgroep en de vijfde als de stikstofgroep. De elementen van de zesde hoofdgroep worden chalcogenen genoemd, die van de zevende hoofdgroep halogenen en de achtste hoofdgroep wordt gevormd door de edelgassen.
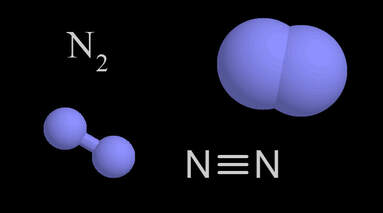
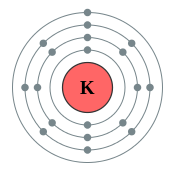
De structuur van de schillen : het waterstofatoom heeft de eenvoudige bouw van alle atomen. In neutrale toestand bestaat het uit één proton, met één elektron in een baan erom heen. Als het water-stofatoom in de grondtoestand is, bevindt dit elektron zich in de eerste schil, die ook wel K-schil wordt genoemd. De atomen van helium, het eerst volgende element, hebben twee protonen in de kern en twee elektronen die zich ook in de K-schil bevinden. Met deze twee elektronen is de K-schil al gevuld en wordt de eerste periode afgesloten. Met litium ( atoomnr. 3 ) begint de opbouw van de tweede schil, de L-schil, en van litium t/m neon wordt er telkens één elektron in de L-schil toegevoegd. Bij neon is ook de L-schil vol, die maximaal acht elektronen kan bevatten.
De eerste hoofdgroep omvat de alkalimetalen ( lithium, natrium, kalium, rubidium, cesium en francium ); de tweede hoofdgroep de aardkalimentalen ( beryllium, magnesium, calcium, strontium, barium, radium ). De derde hoofdgroep wordt aangeduid als de aarden , de vierde als koolstofgroep en de vijfde als de stikstofgroep. De elementen van de zesde hoofdgroep worden chalcogenen genoemd, die van de zevende hoofdgroep halogenen en de achtste hoofdgroep wordt gevormd door de edelgassen.
De structuur van de schillen : het waterstofatoom heeft de eenvoudige bouw van alle atomen. In neutrale toestand bestaat het uit één proton, met één elektron in een baan erom heen. Als het water-stofatoom in de grondtoestand is, bevindt dit elektron zich in de eerste schil, die ook wel K-schil wordt genoemd. De atomen van helium, het eerst volgende element, hebben twee protonen in de kern en twee elektronen die zich ook in de K-schil bevinden. Met deze twee elektronen is de K-schil al gevuld en wordt de eerste periode afgesloten. Met litium ( atoomnr. 3 ) begint de opbouw van de tweede schil, de L-schil, en van litium t/m neon wordt er telkens één elektron in de L-schil toegevoegd. Bij neon is ook de L-schil vol, die maximaal acht elektronen kan bevatten.
|
Iedere schil met het rangnummer n kan ten hoogste 2n2 elektronen opnemen. Dat betekent dat de eerste schil twee elektronen, de tweede schil acht elektronen, de derder schil achttien elektronen en de vierde schil tweeëndertig elektronen kan bevatten. Bij de vijf- zes- en zevende schil wordt de capaciteit om elektronen op te nemen niet meer ten volle benut. Nadat de tweede schil bij het edelgas neon is gevuld, wordt vanaf het alkalimetaal natrium ( atoomnr. 11 ) de derde schil ( de M-schil ) opgevuld; deze periode eindigt voorlopig met acht elektronen bij het edelgas argon. Bij het alkalimetaal kalium ( atoomnr. 9 ), dat op argon volgt, begint de vierde schil ( de N-schil ) zich op te vullen, hetgeen echter bij het element calcium wordt onderbroken. Bij de volgende tien elementen ( van scandium tot zink ), die alle tot nevengroepen behoren, wordt de derde schil, op onregelmatige wijze, opgevuld tot achttien elektronen. Pas bij de volgende groep elementen, vanaf galium, wordt de vierde schil verder opgevuld tot er bij krypton weer een edelgasconfiguratie is bereikt met acht elektronen in de buitenste schil.
|
Elementen met een dergelijke configuratie vertonen weinig chemische activiteiten. De vierde periode omdat in totaal 18 elementen ( waarvan acht in hoofdgroepen en 10 in nevengroepen ).
Op dezelfde wijze als in de vierde periode wordt in de vijfde periode de vijfde schil ( de O-schil ) opgevuld. Ook hier volgt na twee beginelementen ( rubidium en strontium ) een reeks van tien elementen, allemaal in nevengroepen, waarbij de vierde schil tot achttien elektronen wordt opgevuld ( van de tweeëndertig mogelijke plaatsen ). Daarmee omvat ook de vijfde periode achttien elementen.
Op dezelfde wijze als in de vierde periode wordt in de vijfde periode de vijfde schil ( de O-schil ) opgevuld. Ook hier volgt na twee beginelementen ( rubidium en strontium ) een reeks van tien elementen, allemaal in nevengroepen, waarbij de vierde schil tot achttien elektronen wordt opgevuld ( van de tweeëndertig mogelijke plaatsen ). Daarmee omvat ook de vijfde periode achttien elementen.
In de zesde periode begint, na de elementen cesium en barium, de opbouw van de zesde schil ( de P-schil ). Met het daarop volgende lanthaan begint de vijfde schil zich verder op te vullen. De veertien elementen die op lanthaan volgen ( van cerium t/m lutetium ), worden de lanthaniden genoemd; hierin wordt echter eerst de N-schil verder opgevuld tot het maximum van 32 elektronen. Bij het element Hafnium ( atoomnr. 72 ) gaat het opvullen van de O-schil verder, hetgeen voorlopig weer ophoudt bij het element Kwik ( atoomnr. 80 ). Van de elementen Thallium tot en met Radon, alle in hoofdgroepen, wordt de P-schil tot 8 elektronen opgevuld. De zesde periode bestaat daarmee uit 32 elementen ( waarvan 8 in hoofdgroepen, 10 in nevengroepen en 14 lanthaniden ). De opbouw van de zevende schil ( de Q-schil ) in de zevende periode verloopt op vergelijkbare wijze als in de zesde periode. De 14 elementen die op Actiniden ( atoomnr. 89 ) volgen en waarin de vijfde schil wordt opgevuld tot er zich 32 elektronen in bevinden, worden de actiniden genoemd ( van Thorium tot en met Lawrencium ).
|
Van de elementen die in het PSE worden genoemd, komen er 93 in de natuur voor, waarbij wel moet worden opgemerkt dat enkele isotopen van de elementen 93 ( Neptunium ) en 94 ( Plutonium ) in de natuur slechts in zeer kleine hoeveelheden gevormd worden, nl. als vervalproduct van zware Uraniumisotopen. De elementen 95 t/m 109, alsmede het element 43
( Technetium ) kunnen uitsluitend kunstmatig worden vervaardigd met behulp van kernreacties. Van een deel van de elementen met een atoomnummer boven de 100 kunnen op deze wijze maar enkele atomen worden gemaakt. De elementen met atoomgetallen boven de 92 worden de Transuranen genoemd; ze zijn allemaal radioactief en vervallen meestal snel. Doordat de elektronenschillen telkens in dezelfde wetmatige reeksen opgevuld worden, worden ook de chemische en fysische eigenschappen van de elementen door het periodiek systeem bepaald. Aan de basis van alle chemische reacties ligt de neiging van alle atomen om, door het vormen van verbindingen in de energetisch gunstige situatie te geraken waarbij zich 8 elektronen in de buitenste schil bevinden. |
Dit is het geval bij de edelgassen, wat ook de chemische inertie van deze stoffen verklaart. Om deze schil van 8 elektronen te bereiken kunnen atomen elektronen in de schil opnemen, elektronen afgeven of elektronen delen met andere atomen. De elementen uit de eerste, tweede en derde hoofdgroep van het periodiek systeem hebben telkens 1,2 of 3 elektronen in de buitenste schil. Door deze elektronen af te stoten en een- tot driewaardige positieve ionen te vormen, kunnen ze de de configuratie van het edelgas bereiken dat er in het PSE aan voorafgaat. Zo kunnen Natriumatomen, door het afstaan van hetm elektron in de buitenste schil, de edelgasconfiguratie van Neon bereiken, waarbij positieve Natriumionen worden gevormd. Calciumatomen kunnen, door twee elektronen af te staan, de edelgasconfiguratie van Argon bereiken, waarbij tweewaar-dige positieve Calciumionen worden gevormd. De atomen van de elementen in de zesde en zevende hoofdgroep kunnen door het opnemen van elektronen van andere atomen de configuratie bereiken van het edelgas dat er direct op volgt, waarbij een- en tweewaardig negatief geladen ionen worden gevormd. Chloor kan de elektronencon-figuratie van Krypton bereiken door twee elektron op te nemen; daarbij worden negatieve geladen ionen gevormd. Bij de elementen van de vierde en vijfde hoofdgroep worden geen ionen gevormd; deze elementen bereiken de edelgasconfiguratie door elektronen met andere elementen te delen.